Reconnecting injured nerves
(Nature Neuroscience volume 12 | number 9 | SEPTEMBER 2009)

Severed axonal connections do not spontaneously regenerate, creating a major hurdle for functional recovery following spinal cord injury (SCI). Previous attempts to aid axonal regeneration have failed to show correct reinnervation of specific target sites in the brain. On pp. 1106–1113 of this issue, Alto et al. demonstrate the successful anatomical regrowth of rat hind limb sensory nerve into the brainstem, across the SCI site.
The Tuszynski laboratory has previously shown that a combination of local neurotrophin expression, conditioning peripheral nerve injury, and cell grafts applied to and near a lesion site can provoke the partial regrowth of severed sensory axons after SCI. In these experiments, the lentiviral expression of neurotrophin-3 (NT-3) provided the chemoattractive guidance cue to direct regenerating axons. A bone marrow graft at the injury site provided scaffolding, a kind of cellular bridge, for the regenerating nerve tract. Sciatic nerve preconditioning lesions, a manipulation known to promote axonal regeneration, were also used. The regenerating axons grew into and beyond the spinal cord lesion site, but the regenerated axons in these previous studies did not quite reach their original targets in the brainstem.
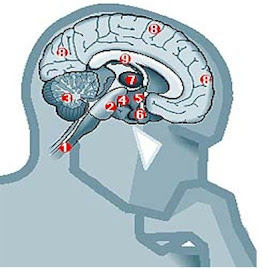
Alto et al. now report ascending sensory tracts that successfully reconnect with their correct target site, the nucleus gracilis in the brain stem. To achieve this, the authors moved the injury site to level C1 on the spinal cord (compared with C4 in their earlier work), where the distance to the target site is much shorter (~2 mm). The picture shows a confocal micrograph oftransganglionic labeling of injured sensory axons (cholera toxin B subunit labeling in red) reaching retrogradely labeled target neurons in the nucleus gracilis (Fluorogold labeling in green). To demonstrate the importance of local neurotrophin gradients in coaxing the regenerating axon to the correct site, the authors misexpressed NT-3 at an inappropriate location, the medullary reticular formation, and found regenerating axons being misdirected and inappropriately reconnected.
Disappointingly, despite this successful anatomical reconnection, these rats did not show appreciable functional recovery. Although regenerating axons formed ultrastructures that are consistent with de novo synaptic contacts, the target neurons in the brain stem showed little or no response to electrical stimulation of the sciatic nerve. Despite the lack of functional recovery, this study shows that proper chemotrophic guidance is a crucial step in promoting recovery after SCI. These findings can potentially aid in designing a combinatorial therapeutic strategy for individuals who have lost peripheral functions as a result of spinal cord trauma.
Min Cho
Chemotropic guidance facilitates axonal regeneration and synapse formation after spinal cord injury
Laura Taylor Alto, Leif A Havton, James M Conner, Edmund R Hollis II, Armin Blesch & Mark H Tuszynski
Nature Neuroscience 12, 1106 - 1113 (2009) Published online: 2 August 2009
doi:10.1038/nn.2365
Interactions between BDNF Val66Met polymorphism and early life stress predict brain and arousal pathways to syndromal depression and anxiety
JM Gatt1,2, CB Nemeroff3, C Dobson-Stone4,5,6, RH Paul7, RA Bryant1,8, PR Schofield4,5,6, E Gordon1,2,9, AH Kemp1,2 and LM Williams1,2
1The Brain Dynamics Centre, Westmead Millennium Institute and University of Sydney at Westmead Hospital, Sydney, NSW, Australia; 2Psychological Medicine, Western Clinical School, University of Sydney, Sydney, NSW, Australia; 3Department of Psychiatry and Behavioral Sciences, Emory University School of Medicine, Atlanta, GA, USA; 4Prince of Wales Medical Research Institute, Sydney, NSW, Australia; 5Medicine, University of New South Wales, Sydney, NSW, Australia; 6Garvan Institute of Medical Research, Sydney, NSW, Australia and 7Behavioral Neuroscience, Department of Psychology, University of Missouri, St Louis, MO, USA; 8School of Psychology, University of New South Wales, Sydney, NSW, Australia and 9The Brain Resource International Database and Brain Resource, Sydney, NSW, Australia and San Francisco, CA, USA
Molecular Psychiatry (2009) 14, 681–695 & 2009 Nature Publishing Group All rights reserved 1359-4184/09 $32.00
NEWS AND COMMENTARY
Environmental influences affecting gene-phenotype relationships: an argument for a causally-based diagnostic entity of Early Life Stress Disorder?
Neurobiological pathways that link gene and environment: early life stress disorder
KRR Krishnan and WD Taylor
Molecular Psychiatry (2009) 14, 681–695 & 2009 Nature Publishing Group All rights reserved 1359-4184/09 $32.00
En estos dos artículos nuevos se menciona la importancia del BDNF en el control de la depresión:
Acute Systemic Fibroblast Growth Factor-2 Enhances Long-Term Extinction of Fear and Reduces Reinstatement in Rats
1School of Psychology, University of New South Wales, Sydney, NSW, Australia
Despite having made substantial advances in the treatment of anxiety disorders over the past few decades it appears that we have now reached a ‘therapeutic impasse’. Further clinical progress requires a greater understanding of the neural mechanisms underlying fear inhibition.
In this study, we examined, for the first time, the effects of fibroblast growth factor-2 (FGF2), a mitogen involved in the molecular cascade of memory, on extinction and relapse in rats. In all experiments, rats were first trained to fear a white noiseconditioned stimulus, and then had this learned fear extinguished the following day.
Extinction is the process underlying exposure-based therapy in humans.
Experiments 1 and 2 demonstrated that FGF2 facilitated the loss of learned fear (ie, extinction) when given either prior to or immediately after extinction but not when given 4 h after extinction.
This suggests that FGF2 must be present during the consolidation of the extinction memory to have an effect.
Experiment 3 further supported this interpretation by showing that short-term extinction must occur for FGF2 to facilitate long-term extinction, suggesting that FGF2 is facilitating the translation of memory from short-term to long-term storage.
In experiment 4 rats given FGF2 immediately after extinction exhibited less shock-induced reinstatement, which is a model preparation of relapse, than did vehicle-treated rats.
Together, these experiments demonstrate that FGF2 facilitates extinction and attenuates relapse.
Thus, FGF2 may be a novel pharmacological adjunct to exposure therapy.
Neuropsychopharmacology (2009) 34, 1875–1882; doi:10.1038/npp.2009.14; published online 18 February 2009
www.neuropsychopharmacology.org
Keywords: fibroblast growth factor-2; fear extinction; reinstatement; rat
1School of Psychology, University of New South Wales, Sydney, NSW, Australia
A pesar de haber realizado importantes avances en el tratamiento de los trastornos de ansiedad en las últimas décadas, parece que ahora hemos llegado a un callejón terapéutico sin salida. Por lo que, para obtener más progresos clínicos, se requiere una mayor comprensión de los mecanismos neurales subyacentes de la inhibición del miedo.
En este estudio, los autores han examinado, por primera vez, los efectos del factor de crecimiento de fibroblastos-2 (FGF2), el cual es un mitógeno que participa en la cascada molecular de la memoria, y en su extinción, así como en su re-establecimiento. En todos los experimentos, las ratas fueron entrenadas para tener miedo, a un estimulo con ruido condicionado, y al siguiente día, aprendieron a extinguir el miedo a ese estimulo.
La extinción de la memoria al miedo es un proceso deseado en la terapia de los seres humanos.
Los experimentos 1 y 2 demostraron que el FGF2 facilitó la perdida del miedo aprendido cuando se administró antes o inmediatamente después de la extinción, pero no cuando se administra 4 horas después.
Esto sugiere que FGF2, tiene que estar presente durante la consolidación de la memoria de la extinción, para que tenga efecto.
El experimento 3 apoyó más esta interpretación, de que el corto plazo de la extinción debe ocurrir para que FGF2 facilite la extinción a largo plazo, lo que sugiere que FGF2 facilita la traducción de la memoria a corto plazo para el almacenamiento de la memoria a largo plazo.
En el experimento 4 a las ratas se les dio FGF2 inmediatamente después de la extinción, reestableciéndose más rápido al choque inducido, lo cual es un modelo de preparación de las recaídas, que se hizo con las ratas tratadas.
En conjunto, estos experimentos demuestran que FGF2 facilita la extinción y atenúa las recaídas.
Por lo tanto FGF2, puede ser un nuevo fármaco adjunto con la terapia.
LEARNING AND MEMORY
The authors generated mice that overexpressed either HDAC1 or HDAC2 specifically in neurons. In Pavlovian fear conditioning tests mice that overexpressed HDAC2 showed impaired associative learning compared with wildtype (WT) mice, whereas HDAC1-overexpressing mice did not differ from WT mice. HDAC2-overexpressing mice also performed worse than WT and HDAC-1overexpressing mice in tests of spatial learning and spatial working memory. Conversely, HDAC2-deficient mice showed the opposite behavioural phenotype.
As synaptic plasticity is assumed to underlie learning and memory, the authors next investigated whether HDAC2 regulates this process. They found that HDAC2-overexpressing, but not HDAC1-overexpressing, mice had lower dendritic spine density and fewer synapses in the hippocampus than WT mice.
HDAC2-deficient mice showed the opposite pattern. Moreover, levels of synaptophysin, a marker for presynaptic terminals, in the CA1 and the amygdala were lower than normal in HDAC2-overexpressors and higher than normal in HDAC2-deficient mice. In addition, high frequency stimulation-induced long-term potentiation in CA1 neurons was impaired in HDAC2-overexpressors and increased in HDAC2-deficient mice. This suggests that HDAC2 negatively regulates synapse formation and synaptic plasticity.
Chromatin immunoprecipitation assays showed that HDAC2 associated (to a greater extent than
HDAC1) with the promoters of genes involved in synaptic plasticity, including the gene that encodes brainderived neurotrophic factor. In the brains of HDAC2-overexpressing mice, the levels of the protein products of these genes were decreased, whereas they were increased in the brains of HDAC2-deficient mice. In addition, in nuclear extracts HDAC2 but not HDAC1 immunoprecipitated with the corepressor COREST (also known as RCOR2), whereas both HDAC1 and HDAC2 co-immunoprecipitated with SIN3A and MTA2. COREST suppresses neuronal gene expression, which may explain why HDAC2 preferentially associates with the promoters of genes involved in synaptic plasticity.
Having shown that HDAC2 negatively regulates synaptic plasticity, spine formation, gene expression and learning and memory, the authors tested whether HDAC2 is a main target of HDAC inhibitors, which can improve memory. They injected the HDAC inhibitor suberoylanilide hydroxamic acid (SAHA) into HDAC2-overexpressing and deficient mice. The treatment normalized contextual fear conditioning and dendritic spine and synapse numbers in HDAC2-overexpressing mice, but had no effect in HDAC2deficient mice.
These findings show that HDAC2, but not HDAC1, modulates synaptic plasticity and suggest that it is a major target for the HDAC inhibitor SAHA. The study opens the door to the development of HDAC2-specific inhibitors that might improve memory in patients with neurodegenerative disorders.
Leonie Welberg
ORIGINAL RESEARCH PAPER Guan, J.-S. et al.
HDAC2 negatively regulates memory formation
and synaptic plasticity. Nature 459, 55–60 (2009)
HDAC2 Es el Número Uno
Las enzimas inhibidoras de la histona deacetilasa (HDAC) se han demostrado que mejoran el aprendizaje y la memoria; sin embargo, existen formas múltiples de HDAC, y el desarrollo del mas efectivo inhibidor de HDAC beneficiaria el conocimiento de estas que participan en la regulación de la plasticidad sináptica. Tsai y sus colegas nos muestran que en las neuronas las HDAC2 son las responsables de la plasticidad sináptica.
Los autores hicieron que ratones generaran una sobre expresión de HDAC1 y HDAC2 específicamente en neuronas. En pruebas de ratones con condiciones de miedo pavloviano, la sobre expresión de HDAC2 mostró una alteración asociativa con el aprendizaje en comparación con ratones de tipo salvajes (TS), mientras que los ratones con sobre expresión de HDAC1 no difiere de los ratones TS. Los ratones con sobre expresión de HDAC2 son peores en las pruebas de la memoria del trabajo en aprendizaje espacial y territorial que los TS y ratones con sobre expresión de HDAC1. Por el contrario, ratones con deficiencia de HDAC2 mostraron un comportamiento contrario.
Como se supone, que la plasticidad sináptica es la base del aprendizaje y la memoria, los autores investigaron si HDAC2 regula este proceso. Encontraron que en la sobre expresión de HDAC2 pero no la sobre expresión de HDAC1, los ratones mostraron menor densidad de espinas dendríticas y menos densidad de sinapsis en el hipocampo que los TS. Los ratones con deficiencia de HDAC2 mostraron todo lo contrario. Además, los niveles de sinaptofisina, un marcador de terminales presinápticos, en
Los ensayos de inmunoprecipitación de cromatina, mostraron que
Habiendo demostrado que, HDAC2 regula negativamente la plasticidad sináptica, la formación de las espinas dendríticas, la expresión génica, la memoria y el aprendizaje, los autores prueban si HDAC2 es un principal objetivo de los inhibidores de HDAC, los cuales pueden mejorar la memoria. Se inyecta ácido hidroxámico suberoilanilida (AHS) que es un inhibidor de HDAC en ratones con sobre expresión y deficiencia de HDAC2. El tratamiento normaliza en condiciones de miedo y el numero de sinapsis y espinas dendríticas en ratones con sobre expresión de HDAC2, pero no tuvo ningún efecto en los ratones que tienen la deficiencia.
Estos resultados demuestran que HDAC2 y no HDAC1 modula la plasticidad sináptica y muestra que es el objetivo principal del inhibidor AHS. Este estudio abre las puertas para el desarrollo de inhibidores específicos de HDAC2, para que se pueda mejorar la memoria en pacientes con trastornos neuro degenerativos.
RESEARCH HIGHLIGHTS
NATURE REVIEWS | DRUG DISCOVERY VOLUME 8 | MAY 2009
Nature Reviews Drug Discovery | AOP, published online 24 April 2009; doi:10.1038/nrd2882
NEURODEGENERAT IVE DISEASE
Rescuing memory
To examine this, they used CX929, an allosteric modulator of a-amino-3-hydroxy-5-methyl 4-isoxazole propionic acid (AMPA)-type glutamate receptors (also known as an ampakine) that increases excitatory transmission and thereby upregulates BDNF expression. When CX929 was injected twice daily for 4 days, HD knock-in mice (CAG140) displayed upregulated hippocampal BDNF levels and robust LTP in hippocampal slices.
Next, the authors tested whether CX929 could reverse the impaired actin polymerization in dendritic spines of the CAG140 mice. Whereas hippocampal slices prepared from vehicle-treated mice showed a low level of labelled dendritic spines in response to neuronal stimulation, CX929 treatment increased the number of densely labelled spines, indicating that CX929 restored activity-driven actin polymerization.
Finally, the authors examined the effects of CX929 treatment on the behaviour of CAG140 mice. In learning tasks, treated mice showed experience-dependent changes in behaviour, and in novel object recognition tests of long-term memory, CX929 reduced long-term memory deficits in the subpopulation of CAG140 mice that had a decreased ability to detect novel objects.
Ampakines are currently undergoing clinical trials for other central nervous system disorders, and seem to be well tolerated. This study provides a rationale for investigating whether such compounds might ameliorate the cognitive defects associated with HD, for which there are currently no treatments.
Charlotte Harrison
et al. Up-regulating BDNF with an ampakine
rescues synaptic plasticity and memory in
Huntington’s disease knockin mice. Proc. Natl
Acad. Sci. USA 5 Mar 2009 (doi:10.1073/pnas.
0811228106)
NEURODEGENERATIVE DISEASE
Rescuing memory
RESEARCH HIGHLIGHTS
NATURE
El Rescate de la Memoria
Un reciente articulo publicado en PNAS a demostrado que la sobre regulación de un factor neurotrofico derivado del cerebro (FNDC), usando un compuesto que modula los receptores del glutamato, mejora las alteraciones de la memoria en un ratón con el modelo de la enfermedad de Huntington (EH).
Para examinar esto, se utiliza CX929, un modulador alostérico de α-amino-3-hidroxy-5-methyl-4-isoxazole propionic acid (AMPA) tipo de receptores de glutamato (también conocido como ampakina) que aumenta la transmisión excitatoria, y por lo tanto sobre regular la expresión de FNDC. Cuando se inyecta CX929 dos veces al día durante cuatro dias, EH en ratones knock (CAG140) demuestra una sobre regulación de los niveles de FNDC hipocampal y grandes PLP en cortes del hipocampo.
Después, los autores probaron si CX929 podría invertir el deterioro de la polimerización de la actina en las espinas dendríticas de los ratones CAG140. Considerando que los cortes del hipocampo de los ratones tratados mostraron un bajo nivel de espinas dendríticas en respuesta a la estimulación neuronal, el tratamiento con CX929 aumento el número de densidad de las espinas, lo que indica que CX929 restaura la actividad impulsada por la polimerización de la actina.
Por ultimo, loas autores examinaron el efecto del tratamiento CX929 n el comportamiento de los ratones CAG140. En tareas de aprendizaje, los ratones tratados mostraron experiencia que dependen en los cambios en el comportamiento, y en la prueba de reconocimiento de nuevos objetos de la memoria a largo plazo, CX929 reduce los déficit de la memoria a largo plazo en la subpoblación de los ratones CAG140, que habían tenido dificultad en la capacidad para detectar nuevos objetos.
Actualmente, se hacen ensayos clínicos con las ampakinas para otros desordenes del sistema nervioso central, y parece que funciona bien. Este estudio, proporciona una justificación para investigar si estos compuestos podrían mejorar los defectos cognitivos asociados con
RESEARCH HIGHLIGHTS
NATURE REVIEWS
| Neuroscience volume 10 | June 2009 Nature Reviews Neuroscience | AOP, published online 13 May 2009; doi:10.1038/nrn2655
Keeping an eye on cell death
MicroRNAs are short, evolutionarily conserved, single-stranded non-coding transcripts that become incorporated into the RNA-induced silencing complex (RISC) to block the translation or induce the degradation of target mRNAs. Recent studies have highlighted their roles in both the development and demise of the nervous system — where they are implicated in the regulation of neurogenesis and the maintenance of synaptic plasticity — and in cancer, where both pro- and anti-apoptotic roles have been described.
Here the authors show that miR-24a is specifically expressed in the retina throughout the development of the eye. Knocking down this microRNA in embryos with an antisense morpholino resulted in a significant reduction in eye size but had no effect on the expression of patterning and differentiation markers or on the number of proliferating cells in the eye. Rather, miR-24a depletion led to an increase in apoptosis, as measured by the number of TUNEL-positive nuclei. Furthermore, the levels of caspase 9 protein were significantly increased in the miR-24a-depleted embryos, whereas caspase 9 mRNA levels were unaffected, suggesting that miR-24a represses caspase 9 translation. Indeed, the authors found that both the caspase 9 and the apaf1 mRNAs contain miR-24a binding sites. Moreover, addition of this microRNA to reporter constructs containing the 3′ untranslated regions of these genes fused to green fluorescent protein confirmed that miR-24a can directly repress their translation.
Together these findings indicate that, by downregulating caspase 9 and apaf1 levels, miR-24a is able to prevent apoptosis in the developing retina, thus helping to ensure normal eye morphogenesis. It is likely that microRNAs exert similar effects in other neural structures that require the levels of proliferating and dying cells to be kept in check.
Monica Hoyos Flight
ORIGINAL RESEARCH PAPER Walker, J. C. &
Harland, R. M. microRNA-24a is required to
repress apoptosis in the developing neural retina.
Genes Dev. 16 Apr 2009 (doi:10.1101/gad.1777709)
MICRORNA
Manteniendo la Vista en la Muerte Celular
La proliferación celular y la muerte celular programada (apoptosis) regulan la forma y el tamaño de los órganos en desarrollo. La apoptosis es particularmente prominente en la formación de la retina, en donde el 90% de las nuevas células ganglionares mueren. Se ha demostrado que las caspasas proapoptóticas son las encargadas de la prevención del sobrecrecimiento en la retina, pero los factores que regulan estas proteínas son desconocidos. Los reportes en Genes and development de Walter y Harland muestran que, el microRNA mir-24a regula negativamente a las caspasa-9 y a la apoptosis factor activador de la proteasa-1 (afap1) y es necesario en la morfogénesis normal del ojo en Xenopus.
Los microRNAs, evolutivamente conservados, de una cadena simple, que se incorporan al complejo de silenciamiento inducido por ARN (RISC) para bloquear el traslado o inducir la degradación del objetivo de los mRNAs. Recientes estudios han destacado el papel, tanto en el desarrollo como en la desaparición del sistema nervioso, donde están implicados en la regulación de la neurogénesis, el mantenimiento de la plasticidad sináptica y en el cáncer en donde se han descrito las funciones pro y antiapoptóticas.
Aquí los autores muestran que mir-24a se expresa específicamente en la retina durante el desarrollo del ojo. Quitando este microRNA en embriones con antisentido morfolino, provoca una reducción significativa en el tamaño de los ojos, pero no tuvo ningún efecto en los patrones de diferenciación y marcadores o en el número de células en la proliferación del ojo. Además, los niveles de la proteína caspasa 9 aumentaron significativamente en los embriones con mir-24a, considerando que los niveles de mRNA caspasa 9 no son afectados, lo que sugiere que mir-24a reprime la codificacion de la caspasa 9. De hecho los autores encontraron que las caspasas 9 y los mRNA apaf1 contienen puentes de unión mir-24a. Además, la adición de este microRNA a regiones de estos genes con fusión de la proteína fluorescente, confirmo que mir-24a reprime directamente su codificación.
En conjunto, estos descubrimientos indican que, por la baja regulación en los niveles de caspasa 9 y apf1, m-24a es capaz de prevenir la apoptosis en el desarrollo de la retina, lo que contribuirá. Es probable que los microRNA ejerzan un efecto similar en otras estructuras neurales que requieran los niveles de proliferación y muerte celular para mantenerse bien.
Abstract
NATURE MEDICINE VOLUME 15 NUMBER 3 PAG 331-337 MARCH 2009
Efectos Neuroprotectores de Factores Neurotróficos del Cerebro en Modelos con la Enfermedad de Alzheimer de Roedores y Primates
Resumen
En la Enfermedad de Alzheimer sucede una profunda disfunción neuronal en la corteza entorrinal de los pacientes, que contribuye a la perdida de memoria a corto plazo. En este estudio se muestran los amplios efectos neuroprotectores de la administración del factor neurotrófico del cerebro (BDNF) en varios animales con el modelo de la enfermedad de Alzheimer, con sus beneficios terapéuticos en el hipocampo afectado. Se insertó el gen de BDNF a ratones transgénicos con tejido amiloide, cuando se administró despues de la aparición de la enfermedad, se recuperó la sinapsis, y normalizó parcialmente la expresión del gen, mejorando la señalización de las células y restaurando tanto el aprendizaje como la memoria. Estos resultados ocurren independientemente de los efectos sobre la placa amiloide. En ratas de edad avanzada, la infusión de BDNF revierte el deterioro cognitivo, mejora las perturbaciones relacionadas con la edad, así como la expresión de genes y restaura la señalización. En ratas y primates adultos, BDNF impide la lesión inducida por la muerte de las neuronas corticales entorrinales. En primates de edad avanzada, BDNF invierte la atrofia neuronal relacionada con la edad y disminuye el deterioro cognitivo. Conjuntamente, estos hallazgos indican que BDNF ejerce importantes efectos sobre la protección fundamental de los circuitos neuronales implicados en la enfermedad de Alzheimer, actuando a través de mecanismos independientes del tejido amiloide.





2 comentarios:
Soy Edgar Solís y estoy en Facebook , vivo cerca de california donde hace 1 año me invitaron a una conferencia de un científico de nombre Dr. Víctor Chávez que según había encontrado la manera de hacer que nuestro cuerpo se auto cure de cualquier problema de salud.
En esta conferencia estuvo el Dr. Israel Díaz quien conto que durante ocho años estuvo cuadripléjico por lesiones en su medula espinal ocasionadas por un accidente de auto. La solución total a su problema fue un compuesto de 16 ingredientes naturales que entre varios cientos de estos, su hijastro el Dr. Chávez (médico general alópata, con varias especialidades neurópatas) y el conocimiento de ellos 2 y 6 científicos más pudieron encontrar a través de la investigación en todos esos años.
Concentrados en el conocimiento de que el cuerpo humano tiene una fábrica de CELULAS MADRE (adultas, no embrionarias) principalmente en la medula ósea y de que estas células podían procrearse y convertirse en cualquier tipo de célula del organismo se dieron a la tarea de buscar entre cientos la combinación ideal para estimularlas, proliferarlas, liberarlas, nutrirlas para que ellas pudiesen hacer óptimamente el trabajo para lo cual fueron diseñadas, o sea crear y de ser necesario regenerar nuestros órganos (como su espina dorsal en este caso, o el cerebro, o cualquier otro, a su estado original).
Actualmente el Dr. Chávez es el presidente de la compañía www.stemvidainternational.com y su página personal es www.victorchavez.org y yo me he convertido en (el distribuidor # 106201) uno de más de los 20,000 actuales de este compuesto 100% natural en capsulas: Stem Alive, puesto que he sido testigo presencial de cientos de diversos casos nunca antes vistos de los cuales varios de ellos video grabados los han subido al YouTube sobre diversos problemas de salud ya resueltos (incluyendo casi todo tipo de los hasta hoy conocidos como incurables o de nacimiento, no importando el tiempo, gravedad o complejidad) y de diversas ciudades donde en solo 2 años de haber salido al público este se está dando a conocer por medio de una red de mercadeo por ser totalmente efectivo y sumamente económico.
Y sabemos que mucha gente no lo cree pero sabemos a la vez que mucha gente lo está probando y logrando su total recuperación en un muy corto tiempo ...por lo que amigos ustedes pueden decidir comprobarlo o no (pues es solamente un suplemento nutricional).
Además de darse la oportunidad como varios la hemos tenido de además obtener la salud hemos obtenido bienestar económico ayudando a que cualquiera haga lo mismo dándoselo a conocer a millones de personas que quieran poner a prueba su fe…Muchas Bendiciones.
informacion de regeneracion de la columna vertebral y mas por medio de activador natural de las celulas madre:
Publicar un comentario